Найти кпд тепловой машины работающей с молями одноатомного идеального газа по циклу
2017-04-24 
Найти КПД тепловой машины, работающей с $\nu$ молями одноатомного идеального газа по циклу, состоящему из адиабатного расширения (1-2). изотермического сжатия (2-3) и изохорного процесса (3-1) (рис.). Работа, совершенная над газом в изотермическом процессе, равна $A$. Разность максимальной и минимальной температур газа в цикле равна $\Delta T$.
Проследим за изменением температуры в этом цикле. При адиабатном расширении (1-2) температура газа уменьшается, поэтому $T_ <2>T_<3>$. Таким образом, максимальная температура в цикле — $T_<1>$, а минимальная достигается на изотерме. Разность между максимальной и минимальной температурами $\Delta T = T_ <1>— T_ <2>= T_ <1>— T_<3>$.
По определению КПД тепловой машины $\eta = \frac
Вычислить работу за цикл $A_<0>$ как площадь фигуры здесь не представляется возможным, так как в школе не изучают уравнение адиабатного процесса. Работу за цикл выразим как сумму работ на отдельных участках: $A_ <0>= A_ <1-2>+ A_ <2-3>+ A_<3-1>$.
В адиабатном процессе (1-2) работа
$A_ <1-2>= — \Delta U = — (U_ <2>— U_<1>) = \frac<3> <2>\nu RT_ <1>— \frac<3> <2>\nu RT_ <2>= \frac<3> <2>\nu R(T_ <1>— T_<2>) = \frac<3> <2>\nu R \Delta T$. Количество теплоты в этом процессе $Q_ <1-2>= 0$.
При изотермическом сжатии (2-3) работа газа отрицательна и равна работе внешних сил над газом, взятой со знаком минус, т.е. $A_ <2-3>= — A$. Количество теплоты на этом участке $Q_ <2-3>= \Delta U + A_<2-3>$, причем $\Delta U = 0$.
Поэтому $Q_ <2-3>= — A 0$, на этом участке газ теплоту получает. Итак, работа за цикл $A_
$\eta = \frac< \frac<3> <2>\nu R \Delta T — A>< \frac<3> <2>\nu R \Delta T> = 1 — \frac<2> <3>\frac< \nu R \Delta T>$
Найти кпд тепловой машины работающей с молями одноатомного идеального газа по циклу
2017-04-24 
Найти коэффициент полезного действия тепловой машины, рабочим телом которой является 1 моль идеального одноатомного газа. Машина работает по циклу, изображенному на рис.: (1-2) — изохора, (3-1) — изобара.
Найдем температуру газа в состоянии (1), используя уравнение Менделеева-Клапейрона:
$p_<0>V_ <0>= RT_ <1>\Rightarrow T_ <1>= \frac
Для состояния (2) получаем: $2p_<0>V_ <0>= RT_ <2>\Rightarrow T_ <2>= \frac<2p_<0>V_<0>>
Тот факт, что $T_ <2>= T_<3>$, вовсе не означает, что (2-3) — изотермический процесс. Из рис. видно, что это — процесс, в котором давление зависит от объема по линейному закону.
Работа газа за цикл численно равна площади прямоугольного треугольника:
Рассмотрим участок (1-2), где $V_ <0>= const$. Используя первый закон термодинамики для этого участка, получаем, что количество теплоты на этом участке
$Q_ <1-2>= \Delta U = U_ <2>— U_ <1>= \frac<3> <2>RT_ <2>— \frac<3> <2>RT_ <1>= \frac<3> <2>R (T_ <2>— T_<1>) = \frac<3> <2>R \left ( \frac<2p_<0>V_<0>>
Рассмотрим участок (2-3). Первый закон термодинамики записывается в виде $Q_ <2-3>= \Delta U + A_<2-3>$ (*).
Изменение внутренней энергии на этом участке
$\Delta U = U_ <3>— U_ <2>= \frac<3> <2>R(T_ <2>— T_<2>) = 0$.
Работа на участке (2-3) численно равна площади трапеции, ограниченной графиком процесса и прямыми $V = V_<0>$ и $V = 2V_<0>$. Итак, $A_ <2-3>= \frac <2p_<0>+ p_<0>> <2>(2V_ <0>— V_<0>) = \frac<3> <2>p_<0>V_<0>$. Подставляя в формулу (*), находим, что $Q_ <2-3>= \frac<3> <2>p_<0>V_ <0>> 0$. И на этом участке газ теплоту получает.
Рассмотрим участок (3-1), где $p_ <0>= const$. Количество теплоты $Q_ <3-1>= \Delta U + A_<3-1>$. Изменение внутренней энергии $\Delta U = U_ <1>— U_ <3>= \frac<3> <2>R(T_ <1>— T_<3>) = — \frac<3> <2>p_<0>V_<0>$.
Найти кпд тепловой машины работающей с молями одноатомного идеального газа по циклу
Чему равен КПД цикла, проводимого с идеальным одноатомным газом? Ответ приведите в процентах, округлить до целых.
КПД тепловой машины определяется как отношение полезной работы и переданного рабочему телу тепла за цикл: Определим сперва полезную работу за цикл, на диаграмме
этой величине соответствует площадь цикла:
Передаваемое газу тепло рассчитаем при помощи первого начала термодинамики:
Рассмотрим последовательно все участки цикла. На участке 1 — 2 газ не совершает работы, а изменение его внутренней энергии (с учетом уравнения Клапейрона-Менделеева) равно:
Так как изменение внутренней энергии положительно, газ получает тепло на этом участке. На участке 2 — 3 газ совершает работу
Изменение его внутренней энергии на этом участке:
Следовательно, на этом участке газ получает тепло
На участке 3 — 1 газ совершает отрицательную работу, он остывает, а значит, его внутренняя энергия уменьшается, следовательно, на этом участке он отдает тепло, а не получает. Окончательно, все полученное газом за цикл тепло равно
Таким образом, КПД цикла равно
А разве здесь не нужно использовать формулу (дельта)U=Q+A, ведь над газом совершают работу, а не газ сам ее совершает. Или как вообще нужно определять в какой задаче какую формулу использовать, разве не нужно ориентироваться по дано задачи?
Формулу можно использовать любую, в зависимости от того, что Вам удобно в данной конкретной задаче. В данной задаче цикл идет по часовой стрелке, следовательно, газ совершает положительную работу, поэтому, возможно, удобнее использовать то, что использовано 🙂
Алексей! Поздравляю Вас. Вы очередной раз «изобрели» вечный двигатель второго рода. Обратите внимание на то, что в условии задачи указано, что газ одноатомный.
Если проделать те же вычисления с двухатомным газом, то значение КПД будет другим, что противоречит первой теореме Карно, которая гласит: «КПД обратимого цикла не зависит от рода вещества, из которого сделано рабочее тело».
Хотелось бы сделать одно замечание по поводу Ваших «тезисов». Один из них гласит: «Квазистатический (протекающий медленно) процесс обратим». Согласно ему, если дизельный двигатель медленно крутить в противоположном направлении, то в топливный бок потечет солярка, а из воздушного фильтра будет выходить очищенный воздух. Ведь, согласно Вашему тезису, все должно возвратиться в исходное положение Неужели Вы поверите этому бреду?!
Мне кажется, этот спор бесконечен. Мой тезис следующий, постараюсь его еще раз передать: «Если на некоторой диаграмме () задана точка, то состояние системы полностью задано и она находится в равновесном состоянии (мы считаем, что уравнение состояния нам известно). Если система не находится в равновесии, то точка на подобных диаграммах вообще не имеет смысла. Далее, когда на диаграмме нарисована линия, это последовательность равновесных состояний, через которые система проходит непрерывно, квазистатически. По линии можно перемещать систему в разных направлениях».
Что касается теоремы Карно, на которую Вы ссылаетесь, мне кажется, что Вы упускаете, существенный факт, что она формулируется для цикла Карно, когда есть нагреватель при одной температуре и холодильник при другой. Для цикла Крно получается все так, как Вы говорите. Но можно придумать огромную кучу оьратимых машин, отличных от машины Карно. Например, можно построить из адиабат и изотерм цикл с тремя температурами. Дальнейшее обобщение дает произвольную кривую. Я Вам уже рассказывал, что любую линию можно построить из адиабат и изотерм. Надеюсь в их обратимости Вы не сомневаетесь.
Ваш пример с двигателем, конечно, не вписывается в эту картину. Процесс превращения топлива в тепло с выбрасыванием продуктов горения нельзя обратить, как ни старайся.
Физика дома
Задача С3 для подготовки к ЕГЭ по физике по теме «Первый закон термодинамики. КПД циклических процессов».
Цикл тепловой машины, рабочим веществом которой является один моль идеального одноатомного газа, состоит из изотермического расширения, изохорного охлаждения и адиабатического сжатия. В изохорном процессе температура газа понижается на ?Т, а работа, совершённая газом в изотермическом процессе, равна А. определите КПД тепловой машины.
Перед решением задачи, необходимо изобразить те процессы, которые происходят с газом на каждом участке. В итоге получается замкнутый цикл, состоящий из изотермы 1-2, изохоры 2-3, адиабаты 3-1.

А для этого расписываем первый закон термодинамики сначала в общем виде, а потом для каждого участка.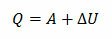

Газ отдаёт теплоту холодильнику на участке 2-3 , на котором идёт изохорное охлаждение газа. Количество теплоты, отданное газом численно равно изменению внутренней энергии на этом участке (работа при изохорном процессе не совершается). Для Q2 =Q23 имеем.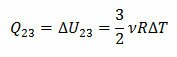
Подставляя Q1=Q12 и Q2= Q23 в формулу для определения КПД и упрощая, получаем итоговый ответ задачи в общем виде.
Внимание! Тексты других задач части С вы можете найти на этой странице.
Задача 30 (5). КПД цикла
Полное условие задачи
Найдите КПД цикла, изображенного на рисунке для идеального одноатомного газа.
Краткое условие задачи
КПД цикла находим по формуле:
где работа определяется как площадь прямоугольника 1234:
Для определения затраченного количества теплоты нужно выяснить, в каких процессах газ получал теплоту. Для этого воспользуемся первым законом термодинамики, формулой для изменения внутренней энергии и уравнением состояния идеального газа:
Рассмотрим каждый процесс по отдельности.
В процессе 1 – 2 начальная температура меньше конечной:
поэтому изменение внутренней энергии больше нуля:
а работа равна нулю, поскольку процесс изохорный:
Отсюда следует, что газ в процессе 1 – 2 получал тепло:
Найдем это тепло:
Разность температур найдем используя уравнение состояния идеального газа. Запишем его для состояния 1 и для состояния 2:
Вычитаем из второго уравнения первое и находим разность температур:
Подставим в формулу для теплоты:
В процессе 2 – 3 начальная температура также меньше конечной:
поэтому изменение внутренней энергии также больше нуля:
а работа в этом процессе больше нуля (газ совершает работу):
поскольку объем увеличивается:
Отсюда следует, что газ в процессе 2 – 3 тоже получал тепло:
Найдем это тепло:
Разность температур найдем используя уравнение состояния идеального газа. Запишем его для состояния 2 и для состояния 3:
Вычитаем из второго уравнения первое и находим разность температур:
Подставим в формулу для теплоты:
В процессе 3 – 4 начальная температура больше конечной:
поэтому изменение внутренней энергии меньше нуля:
а работа равна нулю, поскольку процесс изохорный:
Отсюда следует, что газ в процессе 3 – 4 отдает тепло:
В процессе 4 – 1 начальная температура также больше конечной:
поэтому изменение внутренней энергии также меньше нуля:
работа в этом процессе тоже меньше нуля (над газом совершают работу):
поскольку объем уменьшается:
Отсюда следует, что газ в процессе 4 – 1 тоже отдает тепло:


